Traducción con fines pedagógicos del articulo original de: Brooks GA. Lactate as a fulcrum of metabolism. Redox Biol. 2020 Aug;35:101454 (para ver el original sigue el link)
Se cree erróneamente que es la consecuencia de la falta de oxígeno en la contracción del músculo esquelético, pero ahora sabemos que el enantiómero L del anión lactato se forma en condiciones totalmente aeróbicas y se utiliza continuamente en diversas células, tejidos, órganos y a nivel de todo el cuerpo. Al desplazarse entre las células productoras (impulsoras) y consumidoras (receptoras), el lactato cumple al menos tres propósitos: 1] ser una fuente de energía importante para la respiración mitocondrial; 2] ser el principal precursor gluconeogénico; y 3] ser una molécula de señalización. Trabajando por acción de masa, regulación redox celular, unión alostérica y reprogramación de cromatina por lactación de residuos de lisina en histonas, el lactato tiene influencias importantes en la partición del sustrato energético. El rango fisiológico del [lactato] tisular es de 0,5 a 20 mM y la relación celular lactato / piruvato (L / P) puede oscilar entre 10 y> 500; estos cambios durante el ejercicio y otras respuestas de estrés-tensión eclipsan otras señales metabólicas en magnitud y duración. Por lo tanto, la dinámica del lactato tiene efectos rápidos e importantes a corto y largo plazo sobre la redox celular y otros sistemas de control. Al inhibir la lipólisis en el tejido adiposo a través de HCAR-1 y la captación de ácidos grasos mitocondriales del músculo a través de malonil-CoA y CPT1, el lactato controla la partición del sustrato energético. La exposición repetida al lactato por el ejercicio regular produce efectos importantes sobre la expresión de las enzimas reguladoras de la glucólisis y la respiración mitocondrial. El lactato es el punto de apoyo de la regulación metabólica.in vivo.
Glucólisis; Metabolismo oxidativo; Aerobio; Anaeróbico; Biogénesis mitocondrial; Ejercicio; Gluconeogénesis; Partición del sustrato energético; Señalización célula-célula; Activación SIRT; PPAR-γ; PGC-1α; HCAR1; Lactación de histonas; TGFβ
Se cree erróneamente que es la consecuencia de la deficiencia de oxígeno en la contracción del músculo esquelético, pero ahora sabemos que el enantiómero L del anión lactato se forma en condiciones completamente aeróbicas y se utiliza continuamente en diversas células, tejidos, órganos y a nivel de todo el cuerpo. Por el contrario, el enantiómero D no es típico del metabolismo de los mamíferos y tiene consecuencias negativas que se han descrito anteriormente [ 22 , 49].]. Debido a que en los sistemas de mamíferos el L-lactato es el producto inexorable de una vía metabólica (glucólisis) y el sustrato de otra vía (respiración mitocondrial), el lactato es el vínculo entre las vías glucolítica y aeróbica. En contraste con su descripción inicial como un producto de desecho metabólico y un agente de fatiga, el lactato es el mensajero principal en un sistema de circuito de retroalimentación complejo. De acuerdo con la hipótesis de la lanzadera de lactato, el vínculo entre las células impulsoras de la formación de lactato y las células receptoras de uso o señalización de lactato puede trascender las barreras compartimentales y ocurrir dentro y entre las células, tejidos y órganos [ 14 , 16 , 18 , 19 , 73 , 172 ] ( Figura 1). Los desafíos al suministro de trifosfato de adenosina (ATP) estimulan la producción de lactato, lo que lleva a adaptaciones celulares inmediatas, a corto y largo plazo para apoyar la homeostasis del ATP. La fisiología y bioquímica de este tema fue revisada recientemente y debe ser consultada [ 22 , 49 ], pero posteriormente ha estado disponible nueva información, particularmente con respecto al papel del transporte de lactato en la señalización metabólica [ 85 , 154 , 161 , 176 ].
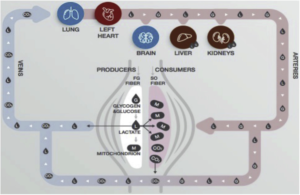
Figura 1. Representación del Láctate Shuttle, que describe las funciones del lactato en el suministro de sustratos oxidativos y gluconeogénicos, así como en la señalización celular. Ejemplos de lanzaderas de lactato célula-célula incluyen intercambios de lactato entre las fibras consumidoras (o receptoras) glicolíticas blancas (FW) y rojo-oxidativas (SO) del productor (o conductor) dentro de un lecho muscular activo y entre el músculo esquelético activo productor y el corazón consumidor, cerebro, hígado y riñones. Entre los ejemplos de lanzaderas de lactato intracelulares se incluyen los intercambios citosol-mitocondrial y citosol-peroxisoma. De hecho, la mayoría, si no todos, los transportadores de lactato son impulsados por un gradiente de concentración o pH, o por un estado redox. Símbolos: G – Glucosa y Glucógeno, L – Lactato y M – elementos del retículo mitocondrial. Compilado originalmente a partir de diversas fuentes (16, 18, 19); de (22).
Como se demostró en todos los sistemas modelo de mamíferos estudiados (ratas, perros, ratones), y principalmente en humanos, a nivel de todo el cuerpo, el metabolismo del lactato cumple al menos tres funciones: 1] el lactato es una fuente de energía importante [ 14 , 37 , 45 , 86 , 105 , 158 , 159 ]; 2] el lactato es el principal precursor gluconeogénico [ 12 , 48 , 110 , 160 ]; y 3] el lactato es una molécula de señalización con efectos autocrinos, paracrinos y endocrinos y se conoce como una “lactormona” [ 16 , 19 , 75]. Los intercambios de lactato dentro y entre las células se denominan lanzaderas de lactato “intracelulares” y “célula-célula” que describen las funciones del lactato en el suministro de sustratos oxidativos y gluconeogénicos, así como un resto de señalización [ 16 , 19 ]. Entre los ejemplos de lanzaderas de lactato intracelulares se incluyen los intercambios citosol-mitocondrial [ 23 , 32 ] y citosol-peroxisoma [ 106 ]. Entre los ejemplos de lanzaderas de lactato célula-célula se incluyen los intercambios de lactato entre las fibras blancas-glucolíticas y rojas-oxidativas dentro de un lecho muscular y entre el músculo esquelético activo y el corazón [ 13 , 62 , 63 ], el cerebro [ 65 , 132 ,164 ], hígado y riñones [ 12 , 48 , 111 , 173 ], astrocitos y neuronas [ 126 ] y viceversa (es decir, neuronas y astrocitos) [ 100 ]. La mayoría, si no todos los transportadores de lactato celular son impulsados por gradientes de concentración o pH, o por estado redox. Sin embargo, numerosos compartimentos y sistemas corporales, como el espacio intersticial, la vasculatura y la circulación, contribuyen al transporte de lactato in vivo.
Recientemente se ha revisado el papel del lactato como fuente de energía combustible preferida para ejercitar los músculos [ 14 , 105 , 108 , 158 ] y como principal precursor gluconeogénico [ 11 , 12 , 48 , 110 , 111 ] [ 22 ]. Por lo tanto, tras una breve revisión del transporte de lactato [ 16 , 19 ], este artículo explora aspectos de la señalización del lactato en la regulación metabólica ( Fig. 2 ).
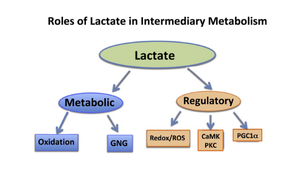
Figura 2. Representación del Láctate Shuttle ya que cumple tres funciones fisiológicas: 1] el lactato es una fuente de energía importante; 2] el lactato es el principal precursor gluconeogénico; y 3] el lactato es una molécula de señalización con efectos de tipo autocrino, paracrino y endocrino y se ha denominado “lactormona”. Estas funciones se pueden subdividir en funciones metabólicas (combustible oxidativo) y gluconeogénicas (GNG) y funciones reguladoras o de señalización
Los supuestos roles del transporte de lactato en la fisiología y el metabolismo continúan ganando apoyo con la investigación en curso [ 37 , 86 , 91 , 161 , 176 ]. En los seres humanos en funcionamiento [ 112 , 113 ], en los músculos esqueléticos humanos en funcionamiento [ 14 , 159 ], así como en los corazones palpitantes de esos individuos [ 13 , 62 , 63 ], se prefiere el lactato a la glucosa y los ácidos grasos como combustible. Se prefiere el lactato a la glucosa como combustible en las preparaciones cerebrales [ 147 , 148 , 150 ] y, lo que es más importante, en los seres humanos.in vivo [ 76 , 164 ]. El transbordador de lactato astrocito-neurona (ANLS) postula que los astrocitos extruyen el lactato y luego las neuronas implicadas en la señalización glutamatérgica lo consumen y oxidan activamente [ 126 ]. Relevante para el transporte de lactato en el cerebro [ 4 , 6 ], las neuronas poseen los componentes celulares necesarios para la captación de glucosa y la producción de lactato, así como para la captación arterial directa de lactato y su uso por un transporte de lactato intracelular [ 74 ]. Además, se ha identificado un papel neuroprotector postraumático del lactato [ 83 , 149 ]. De hecho, debido a que el lactato es el combustible cerebral preferido, normalmente, así como también después de una lesión [ 66, 67 ], se está evaluando la suplementación con lactato para acelerar y mejorar los resultados después de una lesión cerebral traumática (LCT) y otras afecciones [ 103 , 116 , 174 ].
Glucólisis aeróbica y producción y oxidación de lactato : a pesar del efecto Warburg de la glucólisis aeróbica en el cáncer [ 170 ], vide infra , ahora tenemos un buen apoyo que muestra que la glucólisis aeróbica que conduce a la producción de lactato ocurre continuamente en humanos en reposo, así como durante condiciones estresantes como ejercicio, exposición a gran altitud, traumatismos, pancreatitis, sepsis, infarto de miocardio e insuficiencia cardíaca. Al comienzo de esta discusión es importante señalar que el lactato es el producto inexorable de la glucólisis aeróbica ( Fig. 3 ) [ 22 , 139]. Es importante y lamentable que no haya un apoyo experimental sólido para la opinión tradicional de que el flujo glucolítico se dirige a la respiración mitocondrial únicamente a través de la captación de piruvato por el retículo mitocondrial. En el pasado, muchos asumían que el aumento de la abundancia de lactato en el cuerpo indicaba condiciones anaeróbicas a nivel celular, pero nuestra comprensión del lactato como un carbohidrato metabólicamente valioso ha reemplazado esta visión tradicional [ 16 , 49].]. No solo falta apoyo experimental para la noción de que el flujo glucolítico se dirige a la producción de lactato solo cuando falta oxígeno, sino que no hay evidencia de que el primer paso en la oxidación del lactato (es decir, la conversión a piruvato) ocurra en el citosol de cualquier tejido, incluyendo el corazón palpitante o el músculo esquelético activo que tiene una relación de concentración de lactato a piruvato (L / P)> 100 [ 80 ], y que son consumidores netos de glucosa [ 13 ]. Por el contrario, hay pruebas convincentes de que el catabolismo de la glucosa y el glucógeno proceden a la producción de lactato en condiciones totalmente aeróbicas [ 7 , 39 , 136 , 139 ].
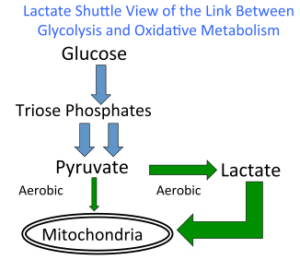
Figura 3. Existe una fuerte evidencia de que el catabolismo de la glucosa y el glucógeno procede a la producción de lactato en condiciones totalmente aeróbicas en estudios en animales intactos, preparaciones de tejido animal y seres humanos sanos in vivo. En los músculos y la sangre arterial de seres humanos sanos en reposo, la concentración de lactato se aproxima a 1,0 mM, mientras que la concentración de piruvato se aproxima a 0,1 mM, siendo el lactato / piruvato (L / P) 10, con producción neta de lactato y liberación del músculo en reposo de individuos sanos cuando se aplica presión parcial intramuscular de oxígeno (PO 2 ) se aproxima a 40 Torr, muy por encima de la PO 2 mitocondrial crítica para la respiración mitocondrial máxima (1-2 Torr) [ 7 , 39 , 140]. Durante el ejercicio, aproximadamente al 65% del consumo máximo de oxígeno (VO 2 máx.), La producción de lactato y la liberación neta de lactato de los lechos musculares activos aumentan y la L / P aumenta más de un orden de magnitud (a ~ 500), pero la PO 2 intramuscular permanece a 3-4 Torr, muy por encima del nivel crítico de O 2 mitocondrial. Por lo tanto, es apropiado concluir que en humanos sanos la glucólisis procede a lactato en condiciones completamente aeróbicas. Es importante señalar que la mayor parte (75 a 80%) del lactato se elimina inmediatamente dentro del tejido o después de su liberación y recaptación por parte del músculo activo, con una captación y oxidación significativas por parte del corazón o la oxidación y el hígado para la gluconeogénesis. Adaptado de diversas fuentes [ 14 , 39 , 80, 136 , 159 ]; de Ref. [ 22 ].
El lactato y el complejo de oxidación del lactato mitocondrial (mLOC) : una inclusión necesaria en el mLOC ( vide infra ) es necesaria porque la controversia rodea el tema de la oxidación del lactato mitocondrial en el metabolismo intermedio. Algunos investigadores han producido preparaciones mitocondriales que oxidan el lactato [ 3 , 15 , 23 , 24 , 27 , 43 , 95 , 125 ], mientras que otros [ 54 , 134 , 143 , 175] han fallado en el intento. Conceptualmente, el problema se resuelve si uno se da cuenta de que el aparato respiratorio celular existe como una red extensa, el retículo mitocondrial [ 93 , 94 ]. Por lo tanto, los intentos de aislar “mitocondrias” para estudios respiratorios ex vivo inevitablemente dan como resultado la interrupción del retículo mitocondrial y la pérdida de funcionalidad [ 64 , 93 ] debido a la labilidad y fragilidad de los constituyentes mitocondriales como el citocromo C y la L-lactato deshidrogenasa (LDH). frente a la homogeneización severa y los detergentes agresivos. Aun así, es posible mostrar oxidación de lactato en preparaciones mitocondriales de mamíferos, incluido el músculo esquelético humano [ 91]. Es importante destacar que la presencia de oxidación de lactato mitocondrial muscular puede demostrarse mediante varias metodologías diferentes, como la espectroscopia de resonancia magnética (MRS) [ 37 , 123 ]. Además, los estudios de células y tejidos musculares que utilizan microscopía de barrido láser confocal, inmunoprecipitación e inmunohistoquímica muestran la presencia de LDH en el complejo de oxidación de lactato mitocondrial [ 73 , 74 ]. Y finalmente, sobre el tema de la oxidación del lactato mitocondrial, amplios estudios en sujetos humanos sanos muestran que la ruta principal de eliminación del lactato es la oxidación [ 14 , 47 , 105 , 108 , [158] , [159] ,[160] ]. En retrospectiva, la incapacidad de algunos investigadores para producir preparaciones mitocondriales que respiran lactato recuerda a estudios previos en los que se utilizaron preparaciones mitocondriales que no lograron oxidar los ácidos grasos de cadena larga. Se encontró que esos resultados fallidos eran atribuibles a la acción de la enzima proteolítica Nagarse [ 122 ]. En ese caso, la incapacidad de las preparaciones de mitocondrias para recapitular lo que se sabe que sucede in vivo puede atribuirse a un artefacto de aislamiento. Lo mismo ocurre con las preparaciones mitocondriales que pierden LDH durante el aislamiento y no pueden oxidar el lactato; esos resultados fallidos se deben a artefactos de aislamiento. La eliminación o paralización de m-LDH en la preparación solo demuestra el papel esencial en la oxidación del lactato mitocondrial in vivo. Y finalmente en este punto, LDH se incluye en las bases de datos de constituyentes mitocondriales, el MitoCarta ( https://www.broadinstitute.org/scientific-community/science/programs/metabolic-disease-program/publications/mitocarta/mitocarta-in-0 ) y MitoMiner ( http://mitominer.mrc-mbu.cam.ac.uk/release-4.0/begin.do ) [ 34 , 121 ]
Gluconeogénesis por lactato : debido a que la mayor parte de la eliminación de lactato se produce por oxidación directa (~ 50% en reposo y 75-80% durante el ejercicio sostenido) [ 14 , 47 ], la discusión anterior sobre la utilización de lactato se centró en la eliminación oxidativa. Sin embargo, mientras que aproximadamente el 25% de la eliminación del lactato se realiza a través de la gluconeogénesis [ 12 , 48 ], el lactato es, con mucho, el principal precursor gluconeogénico [ 61 , 92 ]. El primer reconocimiento de un uso metabólicamente beneficioso del lactato en la fisiología normal fue el descubrimiento del ciclo de Cori con el lactato como el principal precursor gluconeogénico [ 41]. Como se representa típicamente, el ciclo de Cori se representa como si tuviera Transbordadores de lactato intracelular tanto en el músculo como en el hígado, que están unidos a través de un Transbordador de lactato de célula-célula, o más bien un órgano-órgano (músculo a hígado) a través de la vasculatura. Aunque se desarrolló sobre la base de estudios de balance neto de metabolitos en animales de laboratorio, debido a limitaciones técnicas, los Coris no pudieron demostrar el fenómeno en humanos. Afortunadamente ahora, con las mediciones contemporáneas de trazadores isotópicos y de diferencias arteriovenosas, es seguro que la glucemia está respaldada por la gluconeogénesis del lactato durante el reposo postabsorbente (en ayunas) y el ejercicio físico [ 12 , 40 , 48 , 50 , 51 , 92 , 173], y que la función gluconeogénica hepática es aumentada por los riñones en diversas condiciones fisiológicas [ 110 , 111 ].
Trabajo celular, contracción muscular y respiración mitocondrial : los procesos de transducción de energía celular ocurren continuamente, pero en el caso de la contracción muscular, la tasa metabólica aumenta en un orden de magnitud o más [ 22 ]. La hidrólisis de trifosfato de adenosina (ATP) se amortigua inmediatamente por el fosfato de creatina que actúa a través de la creatinfosfocinasa y las tasas de glucólisis y glucogenólisis se ven afectadas por la regulación alostérica de la fosfofructoquinasa, otras quinasas y deshidrogenasas. La concentración de lactato muscular nominal ([lactato]) varía de 0,5 a 1,0 mM, pero el rango dinámico en flujo y concentración puede ser de 20 a 30 veces [ 35 ] con un rango dinámico correspondiente de lactato / piruvato (L / P) de 10 a > 500 [ 80]. Tales cambios drásticos y dinámicos tienen efectos correspondientes sobre la relación celular NAD + / NADH. El aumento de la L / P en sangre durante el ejercicio es relativamente mayor que el aumento relativo de [lactato] porque los incrementos relativos y absolutos de [piruvato] son bajos en comparación con los cambios comparables en [lactato] [ 80 , 171 ]. Por lo tanto, en términos tanto de su rango dinámico absoluto (mM) como del efecto relativo sobre el redox celular, el trabajo celular que conduce a la producción de lactato tiene un efecto enorme en la regulación metabólica tanto en las células receptoras como en las conductoras. A continuación, se muestran otros ejemplos de los efectos de la producción de lactato sobre la redox celular.
Aparte de los principales efectos de la contracción muscular en redox celular [ 68 , 165 ], El L-lactato puede afectar la producción celular de Reactive Oxygen Species (ROS) por ambas reacciones catalizadas enzimáticamente y no enzimáticamente. Quizás, la más conocida es la química por la que se generan ROS como resultado de la respiración mitocondrial [ 124 , 129 ]; menos estudiadas son las interacciones lactato-hierro que son capaces de generar ROS [ 168 ].
Debido a la lanzadera de lactato intracelular, el lactato (no el piruvato) es el principal combustible para la respiración mitocondrial, siempre y particularmente durante el ejercicio cuando la L / P celular aumenta y el orden de magnitud o más (vide supra). Por lo tanto, como principal sustrato de energía mitocondrial y donante de electrones, la respiración celular a corto plazo a partir del lactato aumentará la producción de ROS mitocondrial a través de la actividad de la cadena de transporte de electrones (ETC) [ 75 , 128 , 129 ]. Es importante destacar que, en términos de biogénesis mitocondrial y adaptaciones metabólicas a largo plazo al ejercicio, la exposición al lactato a las células L-6 reguló positivamente muchos genes [ 75 ] (vide infra).
Passarella et al. [ 124 ] descubrieron una segunda forma en la que el metabolismo del L-lactato mitocondrial puede generar ROS, específicamente el peróxido de hidrógeno (H2O2). Utilizando mitocondrias de hígado de rata, demostraron que L-LAC puede generar H2O2 a través de un oxido de lactato (LOX) dependiente de flavina putativa restringida al espacio intermembrana mitocondrial [ 44 ].
Los conceptos de que durante el ejercicio la producción de ROS en las células se apaga y las acciones de las enzimas antioxidantes como el superóxido dismutasa, catalasa, glutatión peroxidasa, otras peroxidasa y enzimas antioxidantes probablemente estén bien cubiertos en los artículos adjuntos de este volumen de simposio. Sin embargo, la idea de la producción de ROS no mediada enzimáticamente proviene de TK Hunt y sus colegas que trabajan en esa área de la cicatrización de heridas [ 88 , 168 ]. Sus hallazgos son que las peroxidasas de fosfato alcalino que contienen hierro de la familia PhoX producen tanto lactato como superóxido. El mecanismo propuesto es que el lactato se quela con el hierro liberado de PhoX produciendo así radicales hidroxilos que rápidamente se descomponen en superóxido. Una consecuencia favorable es que el lactato incita a la liberación de Vascular Endothelial Grecimiento Factor (VEGF), I nterlukin-1 (IL-1), y TGF-β estimular la angiogénesis y la cicatrización de heridas [ 88 ]. Por lo tanto, en opinión de TK Hunt, el lactato puede funcionar como un “preoxidante” en los sitios de la herida (comunicación personal).
Activación de lactato, NAD + y sirtuina : las sirtuinas (SIRT) son una clase de proteínas que se cree que están muy involucradas en la homeostasis celular, incluidos procesos como transcripción, apoptosis, inflamación, resistencia al estrés, biogénesis mitocondrial y eficiencia energética después de la restricción calórica [ 85 , 154 , 161 , 176 ] y envejecimiento [ 36 ]. El nombre proviene de estudios del gen de levadura Regulación silenciosa de información de tipo apareamiento 2. Se conocen siete isoformas de sirtuína (SIRT1-7) y son deacetilasas reguladas por el equilibrio entre nicotinamida (NAM) y NAD +. Se sabe poco sobre los efectos a largo plazo del ejercicio sobre la regulación de la sirtuina, pero se han iniciado estudios de este tipo [ 5 ].
La activación de la sirtuina se logra mediante cambios en el redox celular (es decir, el NAD + / NADH) a través de la concentración de NAM y la actividad de la enzima NAM fosforribosil transferasa (Nampt) que produce NAM. Los cambios sutiles en la redox celular afectan la homeostasis celular, como ocurre en las situaciones mencionadas anteriormente. Sin embargo, faltan datos sobre el cambio en las actividades de Nampt en el músculo activo que impulsa los incrementos de lactato en sangre, así como en los tejidos receptores que no funcionan en los que los cambios en las concentraciones de NAD + y NADH afectan la redox celular in vivo. Sin embargo, como se describió anteriormente, los cambios en la tasa metabólica celular que acompañan al ejercicio dan como resultado efectos similares o mayores sobre el NAD + / NADH celular que cualquier otra perturbación.
Biogénesis mitocondrial y lactato : estudios clásicos en fisiología y bioquímica del ejercicio han demostrado una plasticidad notable del retículo mitocondrial en respuesta a la actividad física regular que puede duplicar la masa mitocondrial [ 42 , 82 , 94 , 137 ]. Los estudios contemporáneos de fisiología y bioquímica también han revelado las señales moleculares de los aumentos inducidos por el ejercicio en la expresión de proteínas mitocondriales. Entre los candidatos de señalización celular para el control transcripcional de la biogénesis mitocondrial se encuentran: Ion calcio [ 119 ], proteína quinasa activada por AMP (AMPK) [ 101 , 167 ], Sirtuin 1 (Sirt1) [ 46 ], Hypoxia Inducible Factor 1α (HIF-1α) [ 152 ], y el ‘activador de la biogénesis mitocondrial maestro,’ Peroxisome receptor activado por proliferadores gamma coactivator- 1α (PGC-1α) [ 72 ]. Reguladores aguas abajo de la biogénesis mitocondrial son: Nuclear RESPIRATORIOS F actores 1 y 2 (NRF-1 y NRF-2), y Mitochondrial Transcription Factor A (TFAM) [ 117]. Lo que estas vías de señalización parecen tener en común son las circunstancias resultantes de un desafío a la homeostasis del ATP [ 17 , 20 , 21 ]. Si bien se ha hecho mayor hincapié en el estudio de los afectos descendentes de la biogénesis mitocondrial (p. Ej., Activación de HIF-1α, AMPK, PGC-1α y PPAR-γ), se ha prestado escasa atención a los afectores ascendentes, como el lactato, como se describe a continuación.
Como se señaló anteriormente, para explicar el resultado de la oxidación del lactato intramuscular e intracelular observado in vivo, postulamos la existencia del mLOC. En un esfuerzo por identificar los componentes del mLOC, [ 75 ] determinamos las respuestas de todo el genoma de las células L6 al L-lactato de sodio exógeno elevado (10 y 20 mM) ( Fig. 4 ). Exposición de lactato aumentó Reactive Oxygen Species (ROS) de producción y hasta regulados-673 genes, muchos conocido por ser sensibles a ROS y Ca ++ ( Fig. 5 ). La inducción de genes que codifican componentes del mLOC se confirmó mediante métodos de reacción en cadena de la polimerasa (PCR) y cambio de movilidad electroforética (EMSA). Transportador de monocarboxilato con aumento de lactato -1 (MCT1) mRNA y las expresiones de proteína dentro de 1 h y Cytochrome c Oxidase (COX) ARNm y proteínas expresión en 6 h de incubación. Los aumentos de COx coincidieron con aumentos en la expresión de PGC1α y la actividad de unión al ADN del NRF-2 nuclear. Entre los otros genes regulados positivamente por el lactato se encuentran las enzimas antioxidantes, como la Glutatión Peroxidasa (GPx), los genes de respuesta al calcio (Ca ++ ) que incluyen la Calcineurina (CaN), la Troponina I de tipo lento (TnI) y la miogenina que son también conocido por responder a CaN y Ca 2+ / Calmodulin dependiente de la proteína k INASE (CaMK). Las ROS pueden aumentar el Ca ++ intracelular que aumenta la actividad de CaMK. Además, el Ca ++ gratuito también puede activar CaMK. Aguas abajo de esas señales son el factor de transcripción cyclic AMP Elemento de respuesta proteína de unión (CREB), Nuclear Factor, Erythroid 2 (NF-E2), Nuclear Factor de kappa promotor de cadena ligera de activadas Bcélulas (NF-kB), y Activator Protein 1 (AP-1).
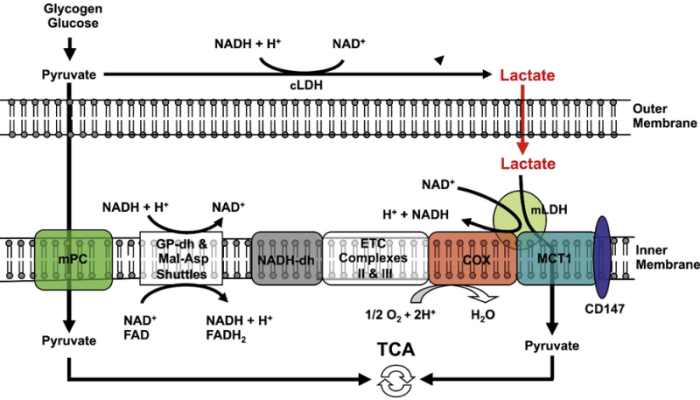
Figura 4. Un esquema que muestra el complejo de oxidación de lactato mitocondrial putativo (mLOC): MCT1 se inserta en la membrana interna mitocondrial interactuando fuertemente con su proteína chaperona CD147, y también está asociada con COX, así como con LDH mitocondrial (mLDH) que podría estar ubicada en el exterior lado de la membrana interna. El lactato, que siempre se produce en el citosol del músculo y otros tejidos debido a la abundancia, actividad y características de la LDH citosólica, se oxida a piruvato a través del complejo de oxidación de lactato en las mitocondrias de la misma célula. Esta reacción de oxidación del lactato endergónico se acopla al cambio redox exergónico en la COX durante el transporte de electrones mitocondrial. Abreviaturas: GP, fosfato de glicerol; Mal-Asp, malato-aspartato; MCT, transportador de monocarboxilato (lactato), mPC, portador de piruvato mitocondrial, ETC, cadena de transporte de electrones; TCA, ácido tricarboxílico; adaptado de Ref. [73 ].
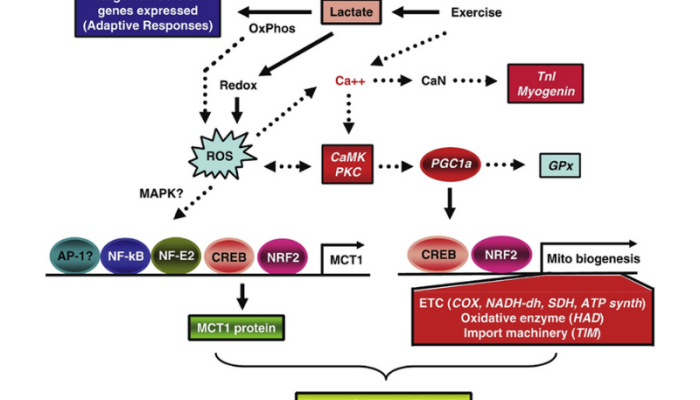
Figura 5. Esquema que resume los efectos del lactato sobre la señalización intracelular en el músculo. Las contracciones estimulan la glucólisis y la posterior producción y acumulación de lactato. En combinación, la acumulación de lactato y la respiración mitocondrial inducen la producción de ROS. Se activa un transcriptoma sensible a ROS, que provoca muchas respuestas celulares observadas en la respuesta al ejercicio, incluida la expresión de MCT1, la biogénesis mitocondrial y la producción de enzimas antioxidantes (p. Ej., GPx). En esta figura, se muestran los nuevos efectos de señalización descritos en el presente informe (flechas continuas). La generación de ROS (lado izquierdo de la figura) es responsable de regular la expresión de MCT1. Para la biogénesis mitocondrial (lado derecho), es probable que la vía de señalización del lactato se fusione con el calcio (Ca ++) que señalan a medida que las contracciones aumentan el flujo de Ca ++ citosólico. Por sí mismo, el lactato aumenta las expresiones de troponina I de tipo lento (TnI) y miogenina que también se sabe que responden al flujo de Ca ++ a través de la calcineurina (CaN). Las ROS pueden aumentar el Ca ++ intracelular que aumenta la actividad de CaMK. Además, el Ca ++ gratuito también puede activar CaMK. El lactato provoca una gran cantidad de respuestas adaptativas, que coordinan el metabolismo como una adaptación funcional al ejercicio en las células del músculo esquelético, como la proliferación del complejo de oxidación del lactato; de Ref. [ 75 ].
Claramente, el lactato puede provocar una gran cantidad de respuestas adaptativas, que coordinan el metabolismo como una adaptación funcional al ejercicio en las células del músculo esquelético, como la proliferación del retículo mitocondrial y el complejo de oxidación del lactato ( Fig. 4 ). En consecuencia, llegamos a la conclusión de que la cascada de señalización de lactato implica la producción de ROS, Ca ++ citosólico y otros factores que convergen en factores de transcripción que afectan la biogénesis mitocondrial. Sin embargo, la señal fisiológica corriente arriba es el lactato que impulsa la adaptación celular al afectar la expresión de cientos de genes.
Lactato y lipólisis en el tejido adiposo: Las relaciones inversas entre la sangre [La –] y la concentración plasmática de ácidos grasos libres [FFA] y la oxidación durante el ejercicio intenso cuando la relación de intercambio de gases ventilatorios (R = VCO 2 / VO 2 ≥ 1,0) se ha reconocido desde hace mucho tiempo [ 31 ], pero se subestiman los mecanismos subyacentes a las asociaciones. En la década de 1960, Issekutz y sus colegas observaron el efecto de la lactacidemia en la disminución de la [FFA] circulante en perros y humanos que realizaban ejercicio intenso [ 90 , 138 ]. Además, la infusión de lactato en perros que corrían hizo que los [FFA] circulantes disminuyesen [ 69 , 90 , 115]. En su trabajo, estos investigadores pudieron observar claramente un efecto del lactato sobre los [FFA] circulantes, pero no se abordó si el mecanismo involucraba iones hidrógeno o aniones lactato, o representaba una inhibición de la lipólisis o una estimulación de la reesterificación de ácidos grasos.
Ahora se sabe que el mecanismo por el cual la lactatemia suprime los FFA circulantes se debe a la supresión de la lipólisis adiposa por parte del lactato que actúa a través de la unión al receptor [ 1 , 33 , 59 , 99 ]. Por otra parte, se sabe ahora que, independientemente de pH o de iones de sodio, inhibe el lactato lipólisis en las células grasas a través de la activación de un receptor acoplado huérfano G-proteína (GPR81), ahora denominado receptor de ácido hidroxicarboxílico 1 (HCAR-1) ( Fig. 6 ). El efecto de la unión del lactato a HCAR-1 parece operar a través de AMP cíclico (cAMP) y CREB [ 9 , 84 , 98 ].
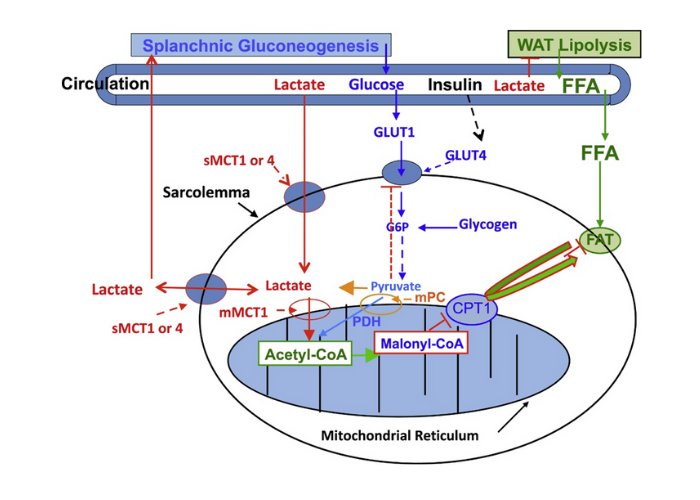
Figura 6 . Ilustración de cómo la lactatemia afecta la captación de glucosa en sangre y periférica, así como la producción, captación y oxidación de FFA dando lugar a inflexibilidad metabólica en el músculo. El lactato es la consecuencia inevitable de la glucólisis [ 139 ], la L / P muscular mínima es 10 y aumenta a una L / P> 100 cuando el flujo glucolítico es alto [ 80]. El lactato es el sustrato oxidable preferido, proporciona inhibición del producto de la oxidación de glucosa y FFA. Como productos de la glucólisis, el lactato y el piruvato proporcionan una inhibición por retroalimentación negativa de la eliminación de glucosa (líneas discontinuas azules). También como sustrato mitocondrial predominante, el lactato da lugar a Acetil-CoA y, a su vez, Malonil-CoA. La acetil-CoA inhibe la β-cetotiolasa y, por lo tanto, la β-oxidación, mientras que la malonil-CoA inhibe la captación del derivado de FFA mitocondrial a través de CPT1 ( T ) [ 142 ]. Además, el lactato es el principal precursor gluconeogénico que aumenta la producción de glucosa y la [glucosa] en sangre (líneas rojas). A través de la unión de GPR81, el lactato inhibe la lipólisis en WAT ( T ) deprimiendo la [FFA] circulante [ 84 , 99]. Este modelo explica la presencia paradójica de lactatemia en ejercicio de alta intensidad y estados de resistencia a la insulina con capacidad limitada para oxidar grasas (líneas verdes). Modificado de Hashimoto et al. [ 74 ]. Abreviaturas: CPT1-Carnitina Palmitoyl Transporter-1, Ácido graso libre de FFA, Translocador de FAT-Ácido graso compuesto por CD36 y FABPc, GLUT-Transportador de glucosa, s-sarcolemmal, m-mitocondrial, Malonil-CoA formado a partir de citrato de TCA exportado controlado por las interacciones de la malonil-CoA descarboxilasa (MCD) y la acetil-CoA carboxilasa (ACC), el transportador MCT-monocarboxilato, el transportador mPC-piruvato mitocondrial, la PDH-piruvato deshidrogenasa, el tejido adiposo blanco WAT, T-Inhibición. No se muestra el Acyl-Co graso (FA-CoA) que se acumulará si los FFA son absorbidos por los miocitos, pero bloqueados de la entrada mitocondrial por el efecto de Malonyl-CoA en CPT1. La FA-CoA intracelular acumulada dará lugar al triglicérido intracelular (IMTG) y la formulación de LC-FA, DAG y ceramidas mediante la inhibición de la PI3 quinasa (PI3-k) y la reducción de la translocación de GLUT4; de Ref. [ 22 ]. (Para la interpretación de las referencias al color en la leyenda de esta figura, se remite al lector a la versión web de este artículo).
Lactato y piruvato como inhibidores de la β-oxidación mitocondrial: como se señaló anteriormente, cuando la glucólisis se acelera durante la contracción muscular, las concentraciones de lactato (L) y piruvato (P) aumentan y aumentan la L / P debido al efecto relativamente mayor sobre el lactato. que [piruvato]. En reposo, la L / P en el efluente muscular y venoso de un lecho muscular se aproxima a 10, pero la relación aumenta más de un orden de magnitud durante el ejercicio de intensidad moderada [ 79 ]. Por acción masiva, el par de monocarboxilato fluye hacia el retículo mitocondrial [ 124 , 142 ], dando lugar a acetil-CoA y, por lo tanto, a la formación de malonil-CoA ( Fig. 6). El aumento de malonil-CoA inhibe la entrada de FFA activados en la matriz mitocondrial inhibiendo la carnitina-palmitoil transferasa-1 (CPT1) [ 107 , 142 ] ( Fig. 6 ). Además, la acumulación de acetil-CoA regula negativamente la β-cetotiolasa, la enzima terminal y limitante de la vía de β-oxidación mitocondrial. Por lo tanto, por acción masiva, la unión alostérica y los efectos sobre el lactato redox celular actúan para cerrar las puertas de los ácidos grasos activados en la matriz del retículo mitocondrial.
Lactato y factor de crecimiento transformante Beta2. Recientemente, un grupo grande, internacional de investigadores han ampliado el conocimiento del papel de la señalización de lactato a través de Transforming Grow Factor BETA 2 (TGF-β2) secretada por adiposo de ejercer ratones [ 161 ]. El TGF-β es una citoquina multifuncional que pertenece a la superfamilia del factor de crecimiento transformante que incluye tres isoformas de mamíferos diferentes (TGF-β1 a -3). Debido a su papel en la regulación y diferenciación de las células madre e inmunes, el TGF-β2 es una citocina muy investigada en los campos del cáncer, enfermedades autoinmunes e infecciosas y las consecuencias de la alteración de la barrera hematoencefálica en la epilepsia, el envejecimiento y TBI [ 53]. Aunque se sabe que todas las isoformas de TGF-β son secretadas por glóbulos blancos, Takahashi et al. demostraron que después del entrenamiento de resistencia, el tejido adiposo de los ratones secretaba TGF-β2 en respuesta a la señalización del lactato. A su vez, TGF-β2 mejoró la tolerancia a la glucosa en ratones, lo que llevó a los autores a concluir que el entrenamiento físico mejora el metabolismo sistémico a través de una comunicación entre órganos (tejido adiposo al hígado) a través de lo que los autores denominaron un “ciclo de señalización lactato-TGF-β2” [ 161 ]. Un papel del lactato que afecta a la señalización de TGF-β2 también se menciona a continuación en la sección sobre biología del cáncer.
En la primera impresión, uno podría pensar que los efectos del lactato inhiben la lipólisis a través de la señalización de HCAR-1 y la oxidación del lactato mitocondrial a través de malonil-CoA ( Fig. 6 ) [ 99 ], por un lado, y aumentan la tolerancia a la glucosa a través de la señalización de TGF-β2 [ 161 ]. , por otro lado, son contradictorios. Sin embargo, una explicación alternativa razonable es que los efectos del lactato sobre HCAR-1 en el tejido adiposo son a corto plazo, agudos como ocurre durante el ejercicio intenso, y que los efectos del TGF-β2 son a largo plazo como ocurre durante la recuperación del ejercicio cuando la tolerancia a la glucosa y la oxidación de lípidos mejoran en hombres y mujeres [ [50] , [51] , [52] , 78]. Si bien los supuestos efectos de la señalización de lactato HCAR-1 y TGF-β2 observados en modelos de roedores esperan validación en humanos, por el momento es seguro que el lactato a corto plazo inhibe la lipólisis y la oxidación de FFA mitocondriales, pero a largo plazo regula positivamente la biogénesis mitocondrial. tolerancia a la glucosa y oxidación de lípidos en humanos in vivo [ 10 , 14 , 51 , 52 , 112 , 113 ].
En un informe reciente, Zhang et al. informó de la regulación de la expresión génica por lactación de 28 residuos de lisina en histonas [ 176]. Las histonas son componentes esenciales de la cromatina, un complejo de ADN y proteínas que regulan la expresión génica. Como se señaló anteriormente con respecto a la regulación redox de las sirtuinas, se sabía que las histonas estaban reguladas por enzimas celulares que agregan o eliminan etiquetas químicas tales como grupos metilo, acetilo o fosfato. Se sabía que esas modificaciones epigenéticas del genoma afectaban procesos como la expresión génica y la replicación y reparación del ADN. Ahora, según los resultados de Zhang et al. la adición de etiquetas de lactato a las histonas es otra forma epigenética por la que se regula el genoma. Y, como se señaló anteriormente, la liberación de lactato de las células impulsoras a la circulación, como ocurre en el ejercicio físico y otras condiciones estresantes, tiene el potencial de afectar la regulación genética en diversas células durante y después del ejercicio físico.
Tan aclamado como los resultados de Zhang et al. son, de alguna manera, los efectos del lactato sobre la expresión génica fueron anticipados por los resultados de investigaciones previas. Por ejemplo, la adición de lactato disminuye el contenido de histona desacetilasa (HDAC) en el núcleo y la actividad de HDAC [ 60 ], así como la metilación y compacidad de la cromatina [ 97 ]. En conjunto, los resultados de estos estudios que sugieren una conformación de cromatina transcripcionalmente permisiva con niveles crecientes de lactato también podrían usarse para respaldar los hallazgos previos de Hashimoto y Brooks sobre un aumento de la unión al ADN tras la adición de lactato a las células L6 [ 75 ].
El trabajo que involucra la regulación epigenética de genes mediante lactación de histonas está en su infancia, pero en el futuro será interesante evaluar los efectos a corto y largo plazo de la lactación de histonas en la biogénesis mitocondrial y la expresión de otras proteínas metabólicas después de ejercicios y regímenes de entrenamiento físico como, así como en diversas enfermedades y afecciones agudas y crónicas como diabetes, sepsis y cicatrización de heridas.
Con base en datos de una variedad de fuentes, se propuso previamente la posibilidad de una lanzadera Gut-Soma Láctate [ 22 ]. El apoyo a la idea se encuentra en el trabajo de Scheiman et al. [ 146 ] quien describió la presencia de microbios intestinales “que mejoran el rendimiento”, miembros del género Veillonella, en las heces de los corredores de maratón. Sus resultados ayudan a reunir evidencia de diversos conjuntos de datos experimentales y epidemiológicos relacionados con la salud intestinal y somática y el rendimiento de los atletas.
Por la ciencia de la nutrición sabemos que los componentes dietéticos prebióticos y probióticos afectan favorablemente la fermentación intestinal y la salud [ 81 ]. Desde la epidemiología sabemos que el ejercicio físico regular es beneficioso para reducir los riesgos de muchos cánceres comunes, incluidos los de colon [ 127 ]. Además, los datos preliminares indican relaciones entre el microbiota y la prevalencia de resistencia a la insulina y síndrome metabólico [ 166 ]. Si bien el entusiasmo es alto, en la actualidad quedan por explorar muchos aspectos de los mecanismos del ejercicio, la función intestinal y la salud.
De sus estudios Scheiman et al. [ 146 ] propuso que el rendimiento de los atletas en la carrera se beneficiaba porque el microbiota intestinal absorbía lactato y lo eliminaba como propionato. Sin embargo, su propuesta es de la “vieja escuela” y le falta el significado del transporte de lactato in vivo. Además, su mecanismo propuesto es poco probable ya que el intestino está subperfundido durante el ejercicio [ 28 ] y el mecanismo sería contraproducente porque durante el ejercicio el lactato se elimina intencionadamente como fuente de energía combustible y precursor gluconeogénico [ 12 ]. Es más probable que ocurra lo contrario, un escenario en el que el intestino suministra lactato, un producto de fermentación que se exporta a través de transportadores de monocarboxilato mediados por sodio (sMCT) [ 38 ,162 ] apoyando así los esfuerzos de los atletas.
Dado el malentendido de larga data sobre el metabolismo del lactato en la ciencia básica, era inevitable que el malentendido se trasladara al tratamiento del paciente en el entorno clínico. Afortunadamente, ahora con la revolución en curso en la comprensión del papel del transporte de lactato en el metabolismo, es de esperar que los médicos utilicen los nuevos conocimientos sobre el metabolismo del lactato y la señalización para mejorar los resultados en personas que sufren enfermedades y lesiones [ 29 , 31 , 58 , 104 ]. ; En la ( Tabla 1 ) se presenta un resumen de las condiciones en las que el tratamiento con lactato puede ser útil . Quizás lo más notable en la Tabla 1 es que el tratamiento con L-lactato se propone para el tratamiento de la sepsis [ 58, 102 ] y cicatrización de heridas y regeneración muscular después de una lesión [ 88 , 118 , 163 ].
Tabla 1. Potencial de tratamiento con lactato para enfermedades y lesiones.
|
Reanimación (líquidos, electrolitos, energía) [ 2 , 57 , 103 ] |
|
Acidosis (la infusión de lactato exógeno tiene un efecto alcalótico) [ 103 , 114 , 174 ] |
|
Regulación de la glucemia (el lactato es el principal precursor de GNG) [ 61 , 104 , 109 , 110 ] |
|
Lesión cerebral traumática (el lactato es combustible cerebral y antiinflamatorio) [ 67 ] |
|
Inflamación (a través de la unión de GPR81, que indica que el lactato inhibe el inflamasoma) [ 84 ] |
|
Pancreatitis aguda y hepatitis (el lactato es un sustrato energético, un precursor de GNG y un agente antiinflamatorio) [ 84 ] |
|
Infarto de miocardio, cirugía cardíaca e insuficiencia cardíaca aguda (el lactato es combustible para el corazón) [ 13 , 153 ] |
|
Quemaduras (el lactato es un sustrato energético, un precursor de GNG y un agente antiinflamatorio) [ 157 ] |
|
Sepsis (la incorporación de lactato en los líquidos de reanimación puede ayudar al mantenimiento de la presión arterial y la circulación, ayudar a administrar antibióticos y sustrato energético, un precursor de GNG y tener un efecto antiinflamatorio) [ 55 , 103 ] |
|
Dengue (el lactato es un sustrato energético, un precursor de GNG y un agente antiinflamatorio) [ 155 , 174 ] |
|
Cognición (el lactato atraviesa fácilmente la barrera hematoencefálica, alimenta las neuronas y estimula la secreción de BDNF, mejora la función ejecutiva y la memoria) [ 77 , 83 , 135 ] |
|
Cicatrización de heridas [ 88 ] y regeneración muscular después de una lesión [ 118 , 163 ]. |
Si bien existe un reconocimiento creciente del papel del transporte de lactato como parte de la fisiología normal, y los médicos están utilizando la terapia con lactato para mejorar los resultados de los pacientes ( Tabla 1 ), hay casos en los que la acumulación y el transporte de lactato pueden ser problemáticos o patológicos. Por ejemplo, en el cáncer, la agresividad de la enfermedad se asocia con el grado de hiperlactatemia [ 71 ]. Existe una larga historia de interés en la producción y acumulación de lactato en la investigación del cáncer (el “Efecto Warburg”) y recientemente los investigadores han intentado inhibir el transporte de lactato en los tumores mediante el bloqueo de los MCT [ 156]. Recientemente, también en el campo de la investigación de la diabetes, los investigadores han tratado de comprender por qué la expresión de MCT se silencia en las células β pancreáticas de manera que no participan en el transporte y la señalización del lactato [ 89 , 120 ]. El silenciamiento de la expresión e inserción de MCT1 en la membrana plasmática es necesario para prevenir la hipersecreción de insulina y la hipoglucemia profunda cuando el lactato sanguíneo es alto y la glucosa en sangre es baja como ocurre en el ejercicio físico. La desregulación del metabolismo del lactato en el cáncer y en los casos en los que la expresión de la proteína MCT de células β no se silencia se ha revisado recientemente [ 22 , 144 ], pero se presenta en forma abreviada a continuación.
Transbordadores de lactato en el metabolismo del cáncer: En 1923, Otto Warburg y Seigo Minami observaron un aumento de la captación de glucosa y una formación excesiva de lactato incluso en condiciones de oxigenación completa [ 169 ]. Efraim Racker [ 133 ] denominó posteriormente el descubrimiento de la glucólisis aeróbica “Efecto Warburg” y, en la actualidad, el fenotipo de alta captación de glucosa / liberación de lactato sigue siendo un sello distintivo del cáncer [ 96 ]. Aun así, aunque el lactato es una gran parte de la biología del cáncer en la actualidad, no hay consenso sobre el significado del efecto Warburg. Nuevamente, en lugar de ser un subproducto de la alta glucólisis en el cáncer, ¿podría la producción de lactato en las células susceptibles al cáncer estar involucrada en la transformación en cáncer? [ 144 ].
En una revisión anterior, Iñigo San Millán y yo describimos a partir de la literatura científica cómo los cánceres lactogénicos, los oncogenes y los factores supresores de tumores mutados parecen comportarse con el aparente propósito de reprogramar la glucólisis para la lactagénesis, creando así gradientes de concentración para el intercambio de lactato dentro, entre y entre las células. [ 144 ]. Las formas en que la lactagénesis puede favorecer la carcinogénesis; estos son: 1) aumento de la captación de glucosa, 2) aumento de la expresión y actividad de la enzima glucolítica, 3) disminución de la función mitocondrial, 4) aumento de la producción, acumulación y liberación de lactato, y 5) regulación positiva de los transportadores de monocarboxilato MCT1 y MCT4 para el intercambio de lactato ( Fig. 7 ).
Como prueba de la hipótesis de la lactagénesis en el cáncer, decidimos reproducir algunos de los primeros estudios de Warburg y asociados, pero con la tecnología moderna de genotipado. Como resultado, San Millán et al. proporcionó datos experimentales en apoyo de la hipótesis de la lactagénesis [ 145]. Usando una línea celular de cáncer humano (células MCF-7), encontramos que tanto el lactato producido de manera endógena como el proporcionado de manera exógena afectaron significativamente la transcripción de oncogenes clave (MYC, RAS y PI3KCA), factores de transcripción (HIF1α y E2F1) y supresores de tumores (BRCA1, BRCA2), así como genes de proliferación y ciclo celular implicados en el cáncer de mama (AKT1, ATM, CCND1, CDK4, CDKN1A, CDK2B). Ciertamente, los resultados de esos estudios deberán replicarse en otros tipos de células cancerosas y biopsias de tumores, pero los resultados sugieren el papel poderoso, pero potencialmente de “espada de doble filo”, del lactato en la regulación metabólica.
Falta de MCT El silenciamiento de MCT de células β pancreáticas puede interferir en la regulación de la glucemia: El mantenimiento de la [glucosa] en sangre es uno de los parámetros esenciales y estrictamente regulados en la fisiología humana. Las interacciones glucosa-insulina son complejas y la interferencia con la glucorregulación, particularmente algo que causa una caída repentina de la [glucosa] en sangre, puede ser desastrosa. La glucosa y el glucógeno son los precursores de la formación de lactato [ 19 , 87 ], y el lactato es el principal precursor gluconeogénico [ 12 , 41 , 48 , 110 , 111]. Sin embargo, mientras que el nivel de glucosa en sangre juega un papel importante en la regulación de su tasa de aclaramiento al influir en los niveles de insulina y hormonas contrarreguladoras, además de proporcionar material precursor para la gluconeogénesis, normalmente el lactato se excluye de los procesos relacionados con la secreción de insulina. Sin embargo, si se permite que ocurra una interferencia con la señalización de glucosa-insulina, el transporte de lactato puede ser perturbador, quizás letal.
Los transportadores de monocarboxilato (lactato) son ubicuos, se expresan en la mayoría de los tejidos [ 16 , 56 , 130 ], incluidos los cánceres [ 151 , 156 ] en los que apoyan el transporte de lactato y actualmente son objetivos de la terapia del cáncer. Anteriormente, se describió en detalle la importancia del lactato en la regulación metabólica. Sin embargo, otra forma de enfatizar la importancia del lactato en la regulación metabólica es por exclusión. Por ejemplo, la deleción embriológica de los transportadores de lactato (MCT) es letal. En términos de glucorregulación in vivo , la importancia del lactato en la glucorregulación se ilustra mediante la exclusión de los MCT de la inserción en las membranas plasmáticas de células β pancreáticas [ 131 , 141]. Allí, la expresión de MCT se silencia para evitar que el lactato extracelular afecte el redox intracelular e interfiera con la detección de glucosa y la secreción de insulina [ 8]. El silenciamiento de MCT1 en las células β pancreáticas es una prueba evolutiva de cómo el lactato anula la glucosa en la regulación de la partición del sustrato energético en general, y la secreción de insulina en particular cuando se debe suprimir el papel dominante del lactato. Es de destacar a este respecto que los individuos que experimentan una supresión fallida de la expresión de MCT de células β pancreáticas se vuelven hipoglucémicos durante el ejercicio intenso que conduce a la lactatemia. Esto se debe a que el lactato accede a las células β pancreáticas y afecta la redox celular como si la glucosa en sangre estuviera elevada. En esos individuos, la entrada aberrante de lactato en las células β pancreáticas provoca la secreción de insulina durante el ejercicio. La combinación de un alto nivel de insulina y una mayor eliminación de glucosa a través del metabolismo provoca una hipoglucemia profunda [ 120 ].
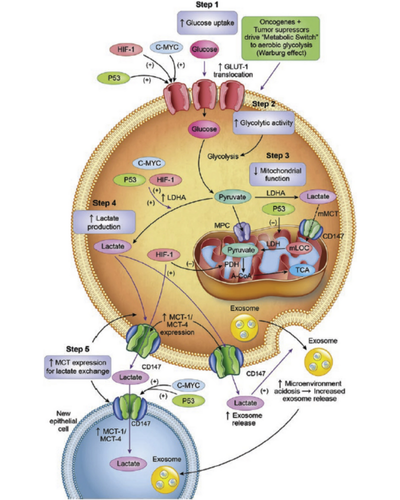
Figura 7. El transporte de lactato salió mal. En el cáncer, el consumo elevado de glucosa que conduce a la producción de lactato en condiciones totalmente aeróbicas (es decir, el efecto Warburg) son características de las células cancerosas y los tumores. La lactagénesis en el cáncer puede verse como un esfuerzo altamente orquestado de oncogenes y mutaciones supresoras de tumores para la utilización continua e ininterrumpida de glucosa para producir lactato que implica 5 pasos principales [ 1 ]: aumento de la captación de glucosa a través de una mayor expresión y translocación de transportadores de glucosa GLUT por transcripción factores Hypoxia-inducible factor 1α (HIF-1) y c-Myc oncogén, así como la pérdida de expresión de tumor factor de supresión de p53 [ 2 ]. Aumento de la expresión y actividad de enzimas glucolíticas, especialmente Lactate Dehidrogenasa A (LDHA) por desregulación de HIF-1α, c-MYC y p53. 3) Disminución de la función mitocondrial principalmente por desregulación de p53 [ 4 ]. Aumento de la producción, acumulación y liberación de lactato debido al efecto de masa de la glucólisis acelerada, disfunción mitocondrial y aumento de la expresión de LDHA. 5) Regulación al alza de los transportadores de monocarboxilato MTC1 y MCT4 y su chaperón de la membrana plasmática, CD147, que contribuye al transporte de lactato desregulado en apoyo de la carcinogénesis; de Ref. [ 144 ].
Ha llegado el momento de pasar la página sobre la comprensión del metabolismo del lactato. Históricamente, cuando se observaron altos niveles de lactato en órganos, tejidos y compartimentos celulares, las observaciones se interpretaron como un estrés para esas células, tejidos y órganos. Lamentablemente, la mala interpretación de las primeras observaciones fue inapropiada y desafortunada porque los eventos observados fueron, de hecho, respuestas de tensión a las tensiones. Por lo tanto, más bien se forma continuamente un producto de desecho del lactato anaeróbico de metabolismo limitado por oxígeno en condiciones totalmente aeróbicas. La velocidad, magnitud y rango de producción de lactato y tasas de acumulación, y las perturbaciones de L / P y redox celular son grandes y fisiológicamente significativas. El transporte de lactato entre las células productoras (impulsoras) y consumidoras (receptoras) cumple al menos tres propósitos: 1] una fuente de energía importante; 2] el principal precursor gluconeogénico; y 3] una molécula de señalización. Como se revisa en este documento, el lactato es el producto inexorable de la glucólisis. En respuesta a la crisis de energía celular, la glucólisis da como resultado la producción de ATP por fosforilación de ADP a nivel de sustrato. También es importante destacar que el lactato (no el piruvato) ingresa al retículo mitocondrial para apoyar la homeostasis de la energía celular mediante la fosforilación oxidativa de ADP y creatina. Cuando la tasa de trabajo celular es alta, el lactato producido por las células conductoras se secreta hacia el intersticio y la circulación, desde donde puede llegar a una variedad de células receptoras, como el corazón, el hígado, los riñones y el cerebro. En diversos tejidos, el lactato actúa por acción de masa, regulación redox celular, generación de ROS, unión alostérica y lactación de histonas. Al inhibir la lipólisis en el tejido adiposo, mediante la unión de HCAR-1 y la activación de CREB, y la captación de ácidos grasos mitocondriales del músculo, a través de malonil-CoA y CPT1, el lactato controla la oxidación de lípidos y la partición total del sustrato energético. La exposición repetida al lactato a partir del ejercicio regular da como resultado procesos de adaptación como la biogénesis mitocondrial y otras características saludables como la mejora de la flexibilidad metabólica. La importancia del lactato y el transporte de lactato en una vida saludable se enfatiza aún más cuando la señalización y el transporte de lactato están desregulados como ocurre en el cáncer y otras afecciones. El lactato es el punto de apoyo de la regulación metabólica. La exposición repetida al lactato a partir del ejercicio regular da como resultado procesos de adaptación como la biogénesis mitocondrial y otras características saludables como la mejora de la flexibilidad metabólica. La importancia del lactato y el transporte de lactato en una vida saludable se enfatiza aún más cuando la señalización y el transporte de lactato están desregulados como ocurre en el cáncer y otras afecciones. El lactato es el punto de apoyo de la regulación metabólica. La exposición repetida al lactato a partir del ejercicio regular da como resultado procesos de adaptación como la biogénesis mitocondrial y otras características saludables como la mejora de la flexibilidad metabólica. La importancia del lactato y el transporte de lactato en una vida saludable se enfatiza aún más cuando la señalización y el transporte de lactato están desregulados como ocurre en el cáncer y otras afecciones. El lactato es el punto de apoyo de la regulación metabólica. in vivo.